6e partie sur les « Régulateurs cellulaires efficaces contre le cancer : grenade, curcuma, brocoli »
- Dans la partie 1, nous avons vu que la grenade, le brocoli et le curcuma sont étudiés dans de nombreuses études cliniques pour leurs effets anti-cancers notamment.
- Dans la partie 2, les effets généraux de la grenade et ses mécanismes d’actions anti-cancers sont évoqués.
- La partie 3 reprend les bienfaits de la grenade (fermentée) dans le cadre des cancers de la prostate, du sein, leucémie, cancer du poumon, de la vessie et du gros intestin.
- La partie 4 s’intéresse aux effets généraux anti-cancers de la curcumine et surtout à sa biodisponibilité.
- La partie 5 s’oriente vers 2 formes de curcumines fortement bio-disponibles et explique leurs propriétés anti-cancers et anti-dépression intéressantes.
Après le grenade fermentée et la curcumine…
Le sulforaphane de brocoli contre le cancer
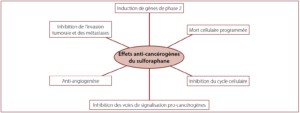
D’autres exemples de substances végétales secondaires présentant des effets protecteurs contre le cancer sont le sulforaphane et les glucosinolates de brocoli. Le brocoli contient du glucoraphane transformé en sulforaphane par l’enzyme myrosinase. De nombreuses études ont démontré que l’utilisation de sulforaphane seul ou associé à d’autres substances naturelles ou médicaments avait eu des effets positifs sur la santé, e.a. un effet anti-cancérigène. Ces substances influenceraient, entre autres, le cycle cellulaire, l’apoptose, l’apparition d’inflammations, la défense antioxydante et les voies de signalisation cellulaire grâce à des mécanismes épigénétiques.
Le groupe de travail formé autour d’Ingrid Herr (clinique universitaire d’Heidelberg et DKFZ) recherche depuis 2007 comment la progression des cellules souches cancéreuses peut être inhibée. Les scientifiques ont découvert que le sulforaphane peut interrompre la voie métabolique – le réseau de signaux NF-kappaB –, rendant les cellules souches cancéreuses inoffensives pour une chimiothérapie.
Associé à un autre cytostatique, le sulforaphane a également un effet cytotoxique sur les cellules souches cancéreuses du pancréas et de la prostate, le sulforaphane renforçant même l’effet du cytostatique. Dans ce cas également, le sulforaphane inhibe le réseau de signaux NFkappaB (Kallifatidis et al., 2011; Rausch et al., 2010).
Outre l’inhibition des facteurs NF-kappaB, d’autres mécanismes permettent au sulforaphane de déclencher des effets protecteurs contre le cancer de la prostate. Une étude sur les cellules cancéreuses prostatiques (Khurana et al., 2016) a montré que le sulforaphane peut être d’une aide utile en cas de blocage hormonal. Le traitement simultané des cellules au moyen de sulforaphane et d’anti-androgènes (bicalutamide, enzalutamide) a permis de renforcer l’effet anti-prolifératif des anti-androgènes et de réduire l’expression du gène PSA.
Les inhibiteurs des HDAC (histone désacétylases) sont des régulateurs épigénétiques et peuvent ainsi influencer le développement du cancer de la prostate. Plus de 20 inhibiteurs des HDAC font actuellement l’objet d’essais cliniques et quatre d’entre eux ont déjà été homologués aux États-Unis pour différents types de cancers. Le sulforaphane est également un inhibiteur prometteur des HDAC (Ganai, 2016).
Le sulforaphane atténue en outre certaines caractéristiques spécifiques des cellules souches du cancer de la prostate et inhibe l’expression du c-myc, un facteur de transcription oncogène. C-myc est une protéine cible importante pour permettre au sulforaphane d’empêcher l’apparition du cancer de la prostate (Vyas et al., 2016).
Pour un essai clinique, 20 patients atteints d’une récidive de cancer de la prostate ont reçu chaque jour un extrait de pousses de brocoli contenant environ 35 mg de sulforaphane pendant max. 20 semaines. Chez sept des participants à ces essais, ce traitement a permis de réduire les valeurs de PSA de 3 à 20 %, voire même de ≥ 50 % chez un autre patient. Si l’on considère tous les participants, le temps de doublement du PSA augmente de manière significative pour passer de 6,1 avant le traitement à 9,6 mois pendant le traitement (Alumkal et al., 2015).
Sur la base de ses essais en laboratoire, le prof. Herr recommande la prise d’une dose de 0,36 mg de sulforaphane par kg, soit 25 mg de sulforaphane par jour pour une personne de 70 kg. Ceci devrait être largement suffisant dans le cadre d’une prévention du cancer. Des doses nettement supérieures de 90 mg de sulforaphane sont cependant utilisées dans des études pilotes en cours sur des patients atteints d’un cancer. Des médicaments contre le cancer à base de sulforaphane sont déjà au stade des tests cliniques.
Biodisponibilité du sulforaphane
Lors de la préparation de brocoli, celui-ci est généralement cuit, ce qui inactive la myrosinase l’empêchant de transformer le glucoraphane contenu en sulforaphane bioactif. La myrosinase est également inactivée dans le cas du brocoli surgelé, blanchi avec congélation. Après la préparation, l’activité est donc finalement quasi nulle (Dosz et Jeffery, 2013). Pour augmenter la teneur en sulforaphane, une astuce simple peut être utilisée : lorsqu’un aliment contenant une quantité suffisante de myrosinase active est consommé avec du brocoli cuit (p.ex. du raifort, du wasabi, des germes de brocoli crus), ceci permet de transformer le glucoraphane du brocoli cuit en sulforaphane et donc de nettement augmenter l’absorption de sulforaphane (Cramer et Jeffery, 2011).
Les germes de brocoli crus contiennent en outre 10 à 100 fois plus de glucoraphane (Fahey et al., 1997) que le brocoli (env. 55 mg par 500 g) (Herr et Büchler, 2010). Les graines, tout particulièrement des plus anciennes sortes de brocoli, sont également particulièrement riches en glucoraphane et sulforaphane. Le germe n’est pas nécessaire ici ; moudre les graines permet déjà de libérer la myrosinase pour former de grandes quantités de sulforaphane.
Dans la prochaine et dernière partie, vous aurez un résumé de ces 6 articles.
Retrouvez tous les articles sur les « Régulateurs cellulaires efficaces contre le cancer : grenade, curcuma, brocoli », en cliquant ici.


















